Struktur Atom
Atom terdiri dari proton, neutron dan elektron. Proton dan neutron berada di dalam inti atom. Sedangkan elektron terus berputar mengelilingi inti atom karena muatan listriknya. semua elektron bermuatan negatif (-) dan semua proton bermuatan positif (+) . sementara itu neutron bermuatan netral. Elektron bermuatan yang bermuatan negatif (-) ditarik oleh proton yang bermuatan positif (+) pada inti atom.
Dalam hal ini, semua atom di alam semesta akan terjadi bermuatan positif (+) karena ada kelebihan muatan listrik positif (+) di dalam proton. Akibatnya, semua atom akan saling bertolak satu sama lain.
A. Perkembangan Teori Atom
- Model Atom Dalton
- Atom merupakan bagian terkecil dari materi yang sudah tidak dapat dibagi-bagi.
- Atom digambarkan sebagai bola pegal yang sangat kecil, suatu unsur memiliki atom-atom yang identik dan berbeda untuk unsur yang berbeda.
- Atom-atom bergabung membentuk senyawa dengan perbandingan bilangan bulat dan sederhana. Misalnya air terdiri atas atom-atom hidrogen dan atom-atom oksigen.
- Reaksi kimia merupakan pemisahan atau penggabungan atau penyusunan kembali dari atom-atom, sehingga atom tidak dapat diciptakan atau dimusnahkan
2. Model Atom Thomson

Atom adalah bola bulat bermuatan
positif dan di permukaan tersebar
elektron yang bermuatan negatif
3. Model Atom Rutherford
Atom adalah bola berongga yang tersusun dari inti atom dan eletron yang tersusun dari inti atom dan e
 lektron
yang mengelilinginya. Inti atom bermuatan positif dan massa atom
terpusat pada inti atom. Kelemahan dari Rutherford tidak dapat
menjelaskan mengapa elektron tidak jatuh ke dalam inti atom. Berdasarkan
teori fisika, gerakan elektron mengitari inti ini disertai pemancaran
energi elektron akan berkurang dan lintasannya makin lama akan mendekati
inti dan jatuh ke dalam inti.
lektron
yang mengelilinginya. Inti atom bermuatan positif dan massa atom
terpusat pada inti atom. Kelemahan dari Rutherford tidak dapat
menjelaskan mengapa elektron tidak jatuh ke dalam inti atom. Berdasarkan
teori fisika, gerakan elektron mengitari inti ini disertai pemancaran
energi elektron akan berkurang dan lintasannya makin lama akan mendekati
inti dan jatuh ke dalam inti.4. Model Atom Niels Bohr
-
- Atom terdiri atas inti yang bermuatan positif dan dikelilingi oleh elektron yang bermuatan negatif di dalam suatu lintasan.
- Elektron dapat berpindah dari satu lintasan ke yang lain dengan menyerap atau memancarkan energi sehingga energi elektron atom itu tidak akan berkurang. Jika berpindah lintasan ke lintasan yang lebih tinggi, elektron akan menyerap energi. Jika beralih ke lintasan yang lebih rendah, elektron akan memancarkan energi lebih rendah, elektron akan memancarkan energi.
- Kedudukan elektron-eletron pada tingkat-tingkat energi tertentu yang disebut kulit-kulit elektron.
B. Menetukan Struktur Atom Berdasarkan Tabel Periodik
1. Partikel Dasar Penyusun Atom
Atom adalah bagian terkecil dari suatu unsur yang masih memiliki sifat unsur tersebut. Struktur atom menggambarkan bagaimana partikel-partikel dalam atom tersusun, atom tersusun atas inti atom dan dikelilingi elektron-elektron yang tersebar dalam kulit-kulitnya. Secara sistematis dapat digambarkan partikel-partikel sub atom berikut.
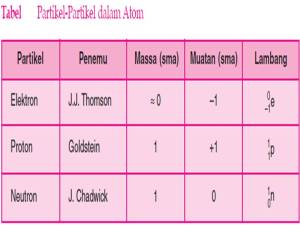
Sebagian besar atom terdiri dari ruang hampa yang dalamnya terdapat inti yang sangat kecil di mana massa dan muatan positifnya dipusatkan dan dikelilingi oleh elektron-elektron yang bermuatan negatif. Inti atom tersusun atas sejumlah proton dan neutron. Jumlah proton dalam inti atom menentukan muatan inti atom, sedangkan massa atom inti ditentukan oleh banyaknya proton dan neutron. Selanjutnya ketiga partikel sub atom (proton, neutron, dan elektron ) dangan kombinasi tertentu membentuk atom suatu unsur yang lambangnya dapat dituliskan :
X : lambang suatu unsur
Z : nomor atom
A : nomor massa
2. Memahami Susunan dari Sebuah Atom
-
- Lihatlah nomor dari tabel periodik. Nomor atom selalu labih kecil dari nomor massa
- Nomor atom merupakan jumlah proton. Oleh karena sifat atom netral, maka nomor atom juga merupakan jumlah elekton
- Susunan elektron-elektron dalam level-level energi, selalu isi level terdalam sebelum mengisi level luar
C. Nomor Atom dan Nomor Massa
Suatu atom memiliki sifat dan massa yang khas satu sama lain. Dengan penemuan partikel penyusun atom dikenal istilah nomor atom (Z) dan nomor massa (A)
Penulisan lombang atom unsur menyetarakan nomor atom dan nomor massa.
Dimana :
A = nomor massa
Z = nomor atom
X = lambang unsur
Nomor Massa (A) = Jumlah proton + Jumlah Neutron
Atau
Jumlah Neutron = Nomor massa – Nomor atom
Nomor Atom (Z) = Jumlah proton
1. Nomor Atom (Z)
Nomor atom (Z) menujukkan jumlah proton (muatan positif) atau jumlah elektron dalam atom tersebut. Nomor atom ini merupakan ciri khas suatu unsur. Oleh karena atom bersifat netral maka jumlah proton sama dengan jumlah elektronya, sehingga nomor atom juga menujukkan jumlah elektron. Elektron inilah yang nantinya paling menentukan sifat suatu unsur. Nomor atom ditulis agak ke bawah sebelum lambang unsur
2. Nomor Massa (A)
Massa elektron sangat kecil dan dianggap nol sehingga massa atom ditentukan oleh inti atom yaitu proton dan neutron. Nomor massa (A) menyatakan banyaknya proton dan neutron yang menyusun inti atom suatu unsur. Nomor massa ditulis agak ke atas sebelum lambang unsur.
E. Isotop, Isobar, dan Isoton suatu Unsur
1. Isotop
Isotop adalah atom yang mempunyai nomor sama tetapi memiliki nomor massa berbeda
Setiap isotop satu unsur memiliki sifat kimia yang sama karena jumlah elektron valensinya sama.
Isotop-isotop unsur ini dapat digunakan untuk menetukan massa atom relatif (Ar) atom tersebut berdasarkan kelimpahan isotop dan massa atom semua isotop
2. Isobar
Isobar adalah unsur-unsur yang memiliki nomor atom berbeda tetapi nomor massa sama.
3. Isoton
Atom-atom yang berbeda tetapi mempunyai jumlah neutron yang sama
D. Menetukan Elektron Valensi
1. Konfigurasi Elektron
Konfigurasi (susunan) elektron suatu atom berdasarkan kulit-kulit atom tersebut. Setiap atom dapat terisi eletron maksimum 2n2, dimana n merupakan letak kulit.
Lambang kulit dimulai dari K, L, M, N dan seterusnya dimulai dari yang terdekat dengan inti atom.
Elektron disusun sedemikian rupa pada masing-masing kulit dan diisi maksimum sesuai daya tampung kulit tersebut. Jadi masing ada sisa elektron yang tidak dapat ditampung pada kulit tersebut maka diletakkan pada kulit selanjutnya.

2. Elektron Valensi
Elektron yang berperan dalam reaksi pembentukan ikatan kimia dan reaksi kimia adalah elektron pada kulit terluar atau elektron valensi.
Jumlah elektron valensi suatu atom ditentukan berdasarkan elektron yang terdapat pada kulit terakhir dari konfigurasi elektron atom tersebut. Perhatikan Tabel untuk menentukan jumlah elektron valensi
Unsur –unsur yang mempunyai jumlah elektron valensi yang sama akan memiliki sifat kimia yang sama pula.